Ma trận đề kiểm tra khảo sát năm học 2013 - 2014 môn: Hóa học 9
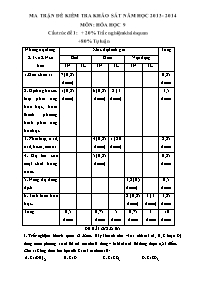
I. Trắc nghiệm khách quan (2 điểm): Hãy khoanh tròn vào 1 chữ cái (A, B, C hoặc D) đứng trước phương án trả lời mà em cho là đúng – Mỗi câu trả lời đúng được 0,25 điểm.
Câu 1: Công thức hóa học của Canxi cacbonat là:
A. Ca(OH)2 B. CaO C. CaCO3 D. CaSO3
Câu 2: Cho 6,5g kẽm vào dung dịch HCl thấy thoát ra V (lít) khí H2 (ở đktc). Giá trị của V là:
A. 4,48 lít B. 2 lít C. 4 lít D. 2,24 lít
Câu 3: Khi làm bay hơi 50g một dung dịch muối thì thu được 0,5g muối khan. Hỏi lúc đầu, dung dịch có nồng độ bao nhiêu phần trăm:
A. 3% B. 1,5% C. 1,1% D. 1%
Bạn đang xem tài liệu "Ma trận đề kiểm tra khảo sát năm học 2013 - 2014 môn: Hóa học 9", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
MA TRẬN ĐỀ KIỂM TRA KHẢO SÁT NĂM HỌC 2013 - 2014 MÔN: HÓA HỌC 9 Cấu trúc đề 1: + 20 % Trắc nghiệm khách quan + 80 % Tự luận Những nội dung KT và KN cơ bản Mức độ đánh giá Tổng Biết Hiểu Vận dụng TN TL TN TL TN TL 1.Điều chế oxi 7 (0,25 điểm) 0,25 điểm 2. Định nghĩa các loại phản ứng hóa học, hoàn thành phương trình phản ứng hóa học 1 (0,25 điêm) 6 (0,25 điểm) 2 (3 điểm) 3,5 điểm 3. Phân loại, oxit, axit, bazơ, muối 4 (0,25 điểm) 1 (2.0 điểm) 2,25 điểm 4. Độ tan của một chất trong nước 5 (0,25 điểm) 0,25 điểm 5. Nồng độ dung dịch 3, 8(0,5 điểm) 0,5 điểm 6. Tính toán hóa học. 2 (0,25 điểm) 3 (3 điểm) 3,25 điểm Tổng 0,5 điểm 0,75 điểm 5 điểm 0,75 điểm 3 điểm 10 điểm ĐỀ BÀI (Mã đề 01) I. Trắc nghiệm khách quan (2 điểm): Hãy khoanh tròn vào 1 chữ cái (A, B, C hoặc D) đứng trước phương án trả lời mà em cho là đúng – Mỗi câu trả lời đúng được 0,25 điểm. Câu 1: Công thức hóa học của Canxi cacbonat là: A. Ca(OH)2 B. CaO C. CaCO3 D. CaSO3 Câu 2: Cho 6,5g kẽm vào dung dịch HCl thấy thoát ra V (lít) khí H2 (ở đktc). Giá trị của V là: A. 4,48 lít B. 2 lít C. 4 lít D. 2,24 lít Câu 3: Khi làm bay hơi 50g một dung dịch muối thì thu được 0,5g muối khan. Hỏi lúc đầu, dung dịch có nồng độ bao nhiêu phần trăm: A. 3% B. 1,5% C. 1,1% D. 1% Câu 4: Cho các dãy chất sau, dãy nào gồm toàn oxit A. K2O, Cu(OH)2, NaCl, SO2 B. CaO, K2O, CaCO3, HCl C. SO 2, CaO, H2SO4, Fe(NO3)3 D. CaO, SO2, Na2O, P2O5 Câu 5: Khi giảm nhiệt độ và tăng áp suất thì độ tan của chất khí trong nước: A. Không tăng và cũng không giảm B. Đều tăng C. Đều giảm D. Có thể tăng và có thể giảm Câu 6: Phản ứng nào sau đây là phản ứng thế: A. SO3 + H2O → H2SO4 B. Fe + 2HCl → FeCl2 + H2 C. 2KClO3 2KCl + 3O2 D. Fe3O4 + 4H2 3Fe + 4H2O Câu 7: Trong các chất sau đây: (1) H2O; (2) KMnO4; (3) KClO3; (4) CaCO3; (5) Không khí. Các chất nào sau đây được dùng để điều chế oxi trong phòng thí nghiệm? A. (2), (3), (5) B. (1), (2), (3) C. (1), (2), (3), (5) D. (2), (3) Câu 8: Hòa tan 336ml khí HCl (đktc) trong 200ml nước. Biết thể tích của dung dịch thay đổi không đáng kể. Nồng độ mol của dung dịch sau khi hòa tan là: A. 0,05M B. 0,075M C. 0,025M D. 0,15M II. Phần tự luận (8 điểm) Câu 1 (2 điểm): Phân loại và gọi tên các chất có công thức hóa học sau: HCl, SO2, CuCl2, NaOH, CaO Câu 2 (3 điểm): Hoàn thành và cân băng các phương trình phản ứng sau: NaOH + H2SO4 .................... + .................... SO2 + CaO .................... Al2O3 + HCl .................... + .................... Na2O + H2O .................... BaCl2 + H2SO4 .................... + .................... Fe + 2HCl ................... + .................... Câu 3 (3 điểm): Cho 3,36 lít khí CO2 (đktc) tác dụng vừa hết với 300ml dung dịch Ba(OH)2, sản phẩm thu được là BaCO3 và H2O a. Viết phương trình phản ứng hóa học xảy ra. b. Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng . c. Tính khối lượng chất kết tủa thu được./. (Cho: Ba = 137; C = 12; H= 1; O = 16; )
Tài liệu đính kèm:
 HOA 9_ MA TRẬN + ĐỀ KTKS _ 01_NĂM 2013 - 2014.doc
HOA 9_ MA TRẬN + ĐỀ KTKS _ 01_NĂM 2013 - 2014.doc





